Resumo dos gases raros (gases nobres) e suas aplicações
Resumo dos gases raros e suas aplicações
O que é um gás raro ou gás nobre?
Gases nobres são os 7 elementos químicos pertencentes ao grupo 18 da tabela periódica, que possuem como característica principal a propriedade de não formar compostos químicos com outros elementos (há raras exceções, como alguns compostos de xenônio), sendo assim basicamente elementos inertes.
Por quê isso acontece? Isso ocorre devido à configuração eletrônica desses elementos: seus átomos possuem a camada de valência completamente preenchida, sem a tendência de aceitar ou doar elétrons para formar ligações químicas.
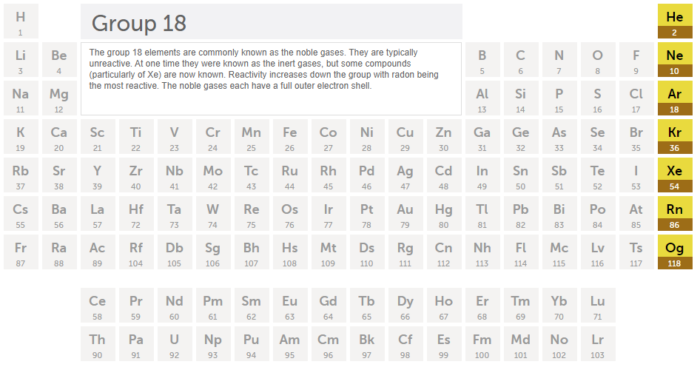
Imagem: Royal Society of Chemistry
Quais são os gases nobres?
Os gases nobres são os seguintes:
- Hélio (He)
- Neônio (Ne)
- Argônio (Ar)
- Criptônio (Kr)
- Xenônio (Xe)
- Radônio (Rn)
- Oganessônio (Og)
Observação: Tanto o gás radônio quanto o oganessônio possuem apenas isótopos radioativos. O oganessônio é um elemento artificial (e na verdade um metal), produzido em ínfimas quantidades em laboratório, e por isso não possui nenhuma aplicação prática até o momento.
Vejamos as principais aplicações desses elementos químicos.
Gases nobres e suas aplicações
| Gás | Z | Símbolo | Aplicações |
| Hélio | 2 | He |
|
| Neônio | 10 | Ne |
|
| Argônio | 18 | Ar |
|
| Criptônio | 36 | Kr |
|
| Xenônio | 54 | Xe |
|
| Radônio | 86 | Rn |
|
Z é o número atômico do elemento.



