Os Domínios da Química
Domínios da Química
Traduzido e adaptado de General Chemistry 1 (Open + Free), Open Learning Initiative
A Química é o estudo da matéria e da energia e suas mudanças. Os químicos estudam e descrevem o comportamento da matéria e da energia em três domínios diferentes: macroscópico, microscópico e simbólico. Esses três domínios da química fornecem diferentes maneiras de considerar e descrever o comportamento químico.
Macro é uma palavra grega que significa “grande”. O domínio macroscópico nos é familiar: trata-se do domínio das coisas cotidianas que são grandes o suficiente para serem detectadas diretamente pela visão ou pelo toque humano. Na vida cotidiana, isso inclui a comida que você come e a brisa que sente em seu rosto. O domínio macroscópico inclui a química diária e de laboratório, onde observamos e medimos propriedades físicas e químicas, ou alterações tais como a densidade, solubilidade e inflamabilidade.
O domínio microscópico da química é quase sempre visitado na imaginação. Micro também vem do grego e significa “pequeno”. Alguns aspectos dos domínios microscópicos são visíveis através de um microscópio, como uma imagem ampliada de um pedaço de grafite ou uma bactéria. Os vírus, por exemplo, são demasiado pequenos para que sejam vistos a olho nu, mas quando estamos resfriados, somos lembrados de como eles são reais.
No entanto, a maioria dos objetos no domínio microscópico da química – como átomos e moléculas – é muito pequena para ser vista, mesmo com microscópios comuns, e muitas vezes deve ser retratada na mente. Outros componentes do domínio microscópico incluem íons e elétrons, prótons e nêutrons e ligações químicas, cada uma das quais é pequena demais para ser vista. Esse domínio inclui os átomos de metal individuais de um fio, os íons que compõem um cristal de sal, as mudanças nas moléculas individuais que resultam em uma mudança de cor, a conversão de moléculas de nutrientes em tecidos e energia e a evolução do calor quando as ligações que conectam átomos juntos são criadas.
O domínio simbólico contém a linguagem especializada usada para representar componentes dos domínios macroscópico e microscópico. Símbolos químicos (como os usados na tabela periódica), fórmulas químicas e equações químicas fazem parte do domínio simbólico, assim como gráficos e desenhos. Também podemos considerar os cálculos como parte do domínio simbólico. Esses símbolos desempenham um papel importante na química porque ajudam a interpretar o comportamento do domínio macroscópico em termos de componentes do domínio microscópico. Um dos desafios para os alunos que aprendem química é reconhecer que os mesmos símbolos podem representar coisas diferentes nos domínios macroscópico e microscópico, e um dos recursos que torna a química fascinante é o uso de um domínio que deve ser imaginado para explicar o comportamento em um domínio que pode ser observado.
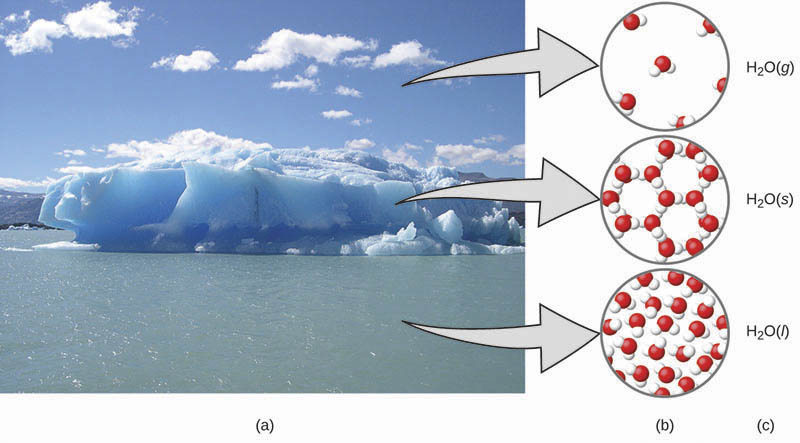
Uma maneira útil de entender os três domínios é através da substância essencial e onipresente que é a água. Que a água é um líquido em temperaturas moderadas, que irá congelar para formar um sólido em temperaturas mais baixas e ferver para formar um gás em temperaturas mais elevadas são observações macroscópicas. Mas algumas propriedades da água caem no domínio microscópico – que não podemos observar a olho nu. A descrição da água, composta por dois átomos de hidrogênio e um átomo de oxigênio, e a explicação do congelamento e da ebulição em termos de atrações entre essas moléculas, estão dentro da arena microscópica. A fórmula H2O, que pode descrever a água nos níveis macroscópico ou microscópico, é um exemplo do domínio simbólico. As abreviações (g) para gás, (s) para sólido e (l) para líquido também são simbólicas.
Observe a imagem a seguir:
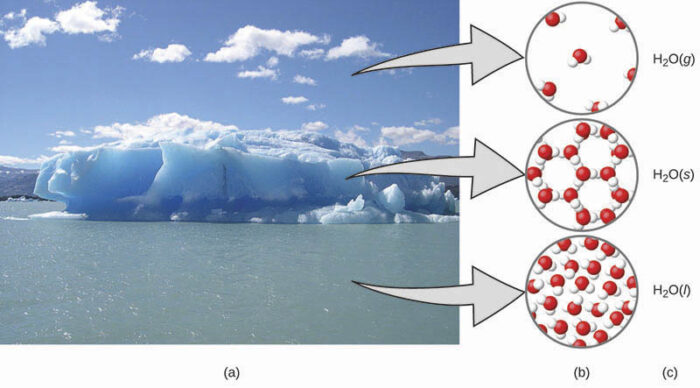
Nesta imagem temos que:
- A umidade no ar, nos icebergs e no oceano representam a água no domínio macroscópico.
- No nível molecular (domínio microscópico), as moléculas de gás estão distantes e desorganizadas, as moléculas de água sólida estão próximas e organizadas, e as moléculas líquidas estão próximas e desorganizadas.
- A fórmula H2O simboliza a água e (g), (s) e (l) simbolizam suas fases (sólida, líquida e gasosa). Observe que as nuvens são realmente compostas por gotículas de água líquida muito pequenas (como o vapor d´água que sai de uma chaleira) ou cristais de água sólida; a água gasosa em nossa atmosfera não é visível a olho nu, embora possa ser percebida como umidade.
Salvo indicação em contrário, este trabalho está licenciado sob Licença Creative Commons Attribution-NonCommercial-ShareAlike 4.0 Unported.
Recomendação de Livro: