Elemento: Mercúrio (Hg)
O Elemento Mercúrio

Descrição
O mercúrio é um metal pesado, de cor branco-prateada, de número atômico 80 na tabela periódica, sendo o elemento que vem logo após o ouro, localizado no grupo 12, 6º período.
É o único metal líquido em temperatura ambiente, sendo um bom condutor de eletricidade – mas não de calor. Se solidifica a -38,83 °C e ferve a 356,73 °C (é bastante volátil), possuindo uma densidade de 13,69 g/cm3 no estado líquido – mais de 13 vezes mais denso que a água!
O símbolo Hg vem da palavra em latim, Hydrargyrum, em si uma forma da palavra hydrargyros em grego antigo. Essa palavra significa “água-prata”, uma alusão ao fato de ser um líquido de cor prateada. O nome mercúrio foi dado pelos antigos romanos em homenagem ao deus Mercúrio, por conta de sua velocidade e mobilidade

História do Mercúrio
O mercúrio é um dos poucos elementos químicos conhecidos desde a antiguidade, sendo encontrado em tumbas egípcias datadas de mais de 1500 anos antes de Cristo. Também era conhecido na Índia, China e Tibete antigos, e foi encontrado até mesmo em uma pirâmide Maia em Teotihuacan, no México, datada de mais de 1800 anos de idade.
Era muito usado pelos antigos gregos para fazer unguentos, na forma de seu principal minério, o Cinábrio. Os romanos o usavam para fabricar cosméticos. O metal já era empregado na fabricação de amálgamas em cerca de 500 a.C., e era conhecido pelos gregos e romanos como minium.
O mercúrio era amplamente usado pelos antigos alquimistas, que o consideravam como uma espécie de material primordial, de onde todos os outros metais eram derivados. Acreditava-se que era possível produzir outros metais misturando mercúrio com enxofre, em proporções variadas, realizando também a transmutação de outros metais em materiais mais nobres, incluindo a produção de ouro – obviamente nada disso é possível.
Aplicações do Mercúrio
O mercúrio encontra diversas aplicações em várias áreas, sendo amplamente usado na fabricação de instrumentos científicos de medição com termômetros, barômetros e manômetros, além de ser empregado em dispositivos eletroeletrônicos como relays, chaves (switches), válvulas, sinais luminosos e lâmpadas fluorescentes e de vapor de mercúrio.
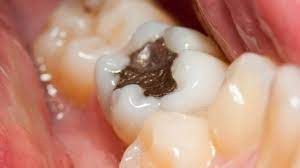
Também é muito utilizado em aplicações de pesquisa científica, na produção de produtos químicos como o hidróxido de sódio e o cloro, e na fabricação de amálgamas (ligas de mercúrio) para restauração dentária. A amálgama para preenchimento dentário é composta geralmente por 52% de mercúrio, 32% de prata e a adição de pequenas quantidades de estanho, cobre e zinco.
Por se ligar facilmente a outros metais, constituindo amálgamas, é empregado também na mineração de ouro e prata, pois dissolve os metais nobres contidos em minérios, permitindo sua fácil extração. Infelizmente esse uso contribui em muito para a contaminação do meio ambiente, principalmente corpos d´água e do solo. É extremamente corrosivo para o alumínio, sendo inclusive proibido seu transporte em aeronaves, por conta do risco de vazamento que pode levar à corrosão de partes da fuselagem!
Também encontra uso como antisséptico e agente antifúngico, na forma de Tiomersal ou Timerosal (C9H9HgNaO2S), que era comercializado pela farmacêutica Lilly com o nome (famoso!) de Mertiolate. Esse produto também pode ser usado como conservante em vacinas e em outros produtos, como testes de alergia e tintas para tatuagens.
Outro antisséptico que também possui mercúrio em sua composição é a Merbromina (C20H8Br2HgNa2O6), conhecida popularmente como Mercurocromo, que atualmente não é mais usado em muitos países, incluindo o brasil, devido à sua alta toxicidade – além do mercúrio, ainda possui em sua molécula átomos de Bromo, outro elemento químico tóxico. O cloreto mercuroso (Hg2Cl2), também conhecido como calomel, é outro antisséptico usado para eliminar microrganismos.
O mercúrio forma diversos compostos úteis combinado com outros elementos. Por exemplo, o cloreto de mercúrio (HgCl2) é um sal (muito venenoso) que já foi bastante empregado para desinfetar feridas. O sulfeto de mercúrio (HgS) é usado desde os tempos antigos para fabricar um pigmento vermelho para tintas chamado vermelhão. Finalmente, o óxido de mercúrio (HgO) é empregado na construção de baterias de mercúrio.
O primeiro uso do mercúrio documentado nas ciências foi no ano de 1644 quando o físico italiano Evangelista Torricelli (1608 – 1647) encheu um tubo de vidro, selado em uma das extremidades, com mercúrio. Ele virou o tudo de cabeça para baixo e o mergulhou em um recipiente cheio de mercúrio, e observou o que acontecia com a coluna de líquido dentro do tubo. Assim, ele foi capaz de “medir” a pressão atmosférica pela primeira vez, criando um barômetro de mercúrio.
Em homenagem a Torricelli, a pressão de 1 mmHg foi chamada de Torricelli (1 mmHg = 1 Torr), mas hoje a unidade de pressão aceita no Sistema Internacional de Unidades – SI é o pascal, Pa, em homenagem ao matemático francês Blaise Pascal (1623 – 1662). 1Torr = 133,3 Pa.
Mineração e Produção do Mercúrio
O mercúrio é um metal raro na crosta terrestre, podendo ser encontrado em forma pura (metal nativo, muito raro), ou em minérios como o cinábrio, esfalerita, corderoíta, livingstonita e outros. O minério mais comum é o cinábrio, um sulfeto de mercúrio de fórmula HgS, que contém 86,21% de mercúrio por peso. O nome cinábrio vem do Persa e significa “sangue de dragão”, uma alusão à sua cor vermelha profunda.
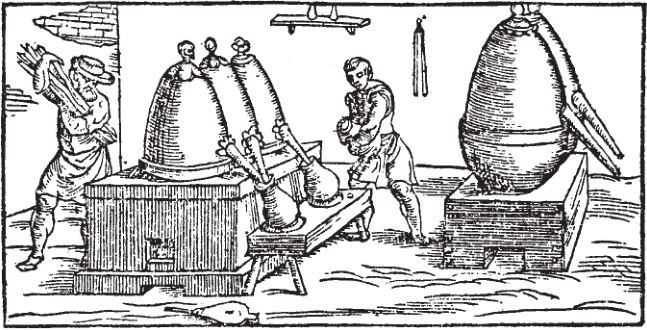
O metal é obtido aquecendo o minério cinábrio em uma corrente de ar e condensando o vapor liberado. As reações envolvidas no processo são:
2HgS + O2 → 2HgO + 2SO2
Nesta etapa são formados dióxido de enxofre e óxido de mercúrio, que na próxima etapa se decompõe espontaneamente na temperatura em que ocorre a reação, liberando gás oxigênio e deixando para trás o mercúrio metálico:
2HgO → 2Hg + O2
Historicamente a maior produção de mercúrio veio da Itália e da Espanha (mais da metade da produção mundial), mas atualmente os maiores produtores mundiais do metal são a China, o Quirguistão, Rússia, Chile e Tadjiquistão. A mina de Almadén (Sisapo, na antiguidde) na Espanha operou de forma contínua desde 400 a.C. até alguns poucos anos atrás.
Acredita-se que vários países produzam mercúrio a partir de processos industriais de separação eletrolítica do cobre, e por recuperação a partir de efluentes, sem no entanto registrar essa produção.
Papel Biológico e Toxicidade do Mercúrio
O mercúrio não possui papel biológico em animais, incluindo seres humanos, e na verdade pode ser extremamente tóxico se ingerido, principalmente na forma de sais ou compostos orgânicos (organometálicos), ou se seus vapores forem inalados, podendo causar intoxicações graves, problemas neurológicos e até mesmo a morte. O metal age como um veneno cumulativo, e níveis perigosos podem ser atingidos em um organismo a partir da exposição contínua. Isso ocorre comumente na cadeia alimentar marinha, onde peixes contaminados por mercúrio são consumidos por peixes maiores, e assim sucessivamente, até que sejam consumidos por seres humanos, podendo se acumular no nosso organismo também e causar doenças graves.
O metal pode inclusive ser absorvido pela pele, e portanto seu manuseio deve ser feito com muita cautela e usando EPIs adequados.
O metal vem sendo gradativamente substituído em muitas de suas aplicações por materiais menos tóxicos. Por exemplo, termômetros de mercúrio tem sido fabricados com uma liga denominada Galinstan, que consiste numa mistura menos tóxica dos metais Gálio, Índio e Estanho, que funde a -19 °C, mesmo essa liga tendo um custo mais elevado que o mercúrio em si.
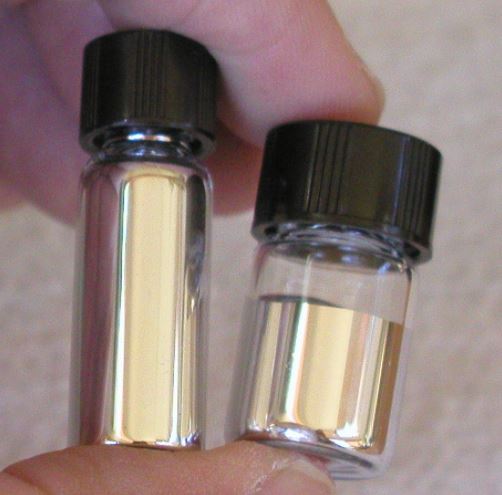
Curiosidades sobre o Mercúrio
Todos os elementos conhecidos na Antiguidade são citados na Bíblia em algum ponto, exceto o mercúrio, apesar dele já ser conhecido por pelo menos três séculos antes de Cristo, sendo mencionado pelo filósofo grego Aristóteles, que o chamava de “prata fluida”.
O mercúrio é classificado como um elemento calcófilo, termo que indica que um elemento tem grande afinidade pelo enxofre e outros calcogênios que não o oxigênio (elementos do grupo 16 na tabela periódica), e que são encontrados próximo à superfície da Terra.
Apesar do mercúrio ser o único metal líquido em temperatura ambiente, outros dois metais são quase líquidos, dependendo da estação do ano em que nos encontramos! São eles o Gálio, que se funde a aproximadamente 30 °C, e o Césio, que se funde a cerca de 28 °C. Ou seja, em um dia quente de verão, três metais são líquidos na temperatura em que o ambiente se encontra.

Mineração de ouro
Um dos processos mais antigos de separação do ouro é o processo de amalgamação. Esse processo se baseia no fato de que o mercúrio forma ligas metálicas facilmente com alguns outros metais, principalmente com o ouro.
Nos tempos dos antigos Romanos o minério cinábrio, encontrado na Espanha e outras regiões do Mediterrâneo, era empregado para obtenção do mercúrio por meio de destilação. O mercúrio assim obtido era misturado com minério de ouro triturado, e a amálgama formada era retirada da mistura. Logo após, a amálgama era destilada, com o mercúrio evaporando e deixando para trás o ouro puro. O mesmo era feito com a extração de prata e platina.
Não é necessário ressaltar que esse é um método inacreditavelmente perigoso de extração do ouro, por envolver a criação deliberada de grandes quantidades de vapor quente de mercúrio. E essa técnica foi extensivamente usada pelos espanhóis no Novo Mundo, que forçavam os Incas e outros nativos do Peru, Bolívia e outros locais na América do Sul a trabalharem no “refino” do ouro e prata – e deixando muitos mortos no processo.
Dados Gerais:
- Símbolo: Hg
- Número Atômico: 80
- Massa Atômica: 200,592
- Ponto de Fusão: -38,83 °C / 234,32 K
- Ponto de Ebulição: 356,73 °C / 629,88 K
- Densidade: 13,5336 g/cm3
- Abundância Estimada na Crosta Terrestre: 8,5×10-2 mg/kg
- Abundância Estimada nos Oceanos: 3×10-5 mg/L
- Número de Isótopos Estáveis: 7
- Energia de Ionização: 10,438 eV
- Estados de Oxidação: +1, +2
- Raio atômico (Van der Waals): 209 pm
- Configuração Eletrônica:
1s2 2s2 2p6 3s2 3p6 3d10 4s2 4p6 4d10 4f14 5s2 5p6 5d10 6s2
Referências
- Emsley, J. Nature´s Building Blocks: An A-Z Guide to the Elements. 1ª Edição. 2001. Oxford University Press
- Enghag, P. Encyclopedia of the Elements. 1ª ed. 2004. Wiley-VCH
- Gray, T. The Elements – A Visual Exploration of Every Known Atom in the Universe. 1ª Edição. 2009. Black Dog & Leventhal Publishers.
- Green, D. The Periodic Table in Minutes: The elements and their chemistry explained in an instant. 1ª Edição. 2016. Ed. Quercus
- Jackson, T.; Challoner, J. The Periodic Table Book – A Visual Encyclopedia of the Elements. 1ª Ed. 2017. Dorling Kindersley Ltd.
- PubChem. Mercury. https://pubchem.ncbi.nlm.nih.gov/element/80. National Library of Medicine.




Pingback: Tipos de Ligas de Prata e suas Aplicações - Diário Numismático
Pingback: Tipos de Ligas de Prata e suas Aplicações - Diário do Naturalista